Que são cromossomos?
Os cromossomos carregam o genético material a organismo (réácido eoxirribonucleico, DNA) Existem 23 pares de cromossomos nas células humanas. Esses cromossomos carregam toda a informação genética de cada célula para funcionar corretamente.
Anormalidades cromossômicas podem causar uma variedade de distúrbios genéticos que podem levar a atraso no desenvolvimento, congênito defeitos e função corporal anormal [2].
Essas doenças genéticas podem ocorrer devido à perda ou ganho de cromossomos ou há deleções ou duplicações de um cromossoma. Nesses casos, a célula específica está ausente genes portanto, não pode produzir certas proteínas e desempenhar corretamente sua função. Exemplos relevantes de dermatologia incluir:
-
Baixa síndrome (trissomia 21)
-
Síndrome de Turner (cromossomo X funcional único)
-
Síndrome de DiGeorge.
O que é citogenético testes?
Citogenética é o estudo dos cromossomos e sua estrutura. [1].
O teste citogenético envolve a análise de células em uma amostra de sangue, tecido, amniótico líquido, medula óssea ou cérebro vascular fluido para identificar quaisquer alterações nos cromossomos de um indivíduo.
Existem 3 métodos principais de teste citogenético.
- Cariótipo de rotina
- Fluorescente no lugar hibridação (PEIXE)
- Hibridação Genômica Comparada (CGH) e microarrays hibridação genômica comparativa (aCGH)
Cariótipo
O cariótipo foi um dos primeiros métodos de análise cromossômica. Este método usa luz microscopia e procedimentos padronizados de coloração em células na porção metafásica do ciclo celular, quando os cromossomos são mais condensados [3].
Para fazer o cromossômico Para uma análise mais eficaz e eficiente, foram desenvolvidos pontos para ligar o DNA e produzir padrões de bandas característicos para identificar diferentes cromossomos [3]. A mancha mais usada é a mancha Giemsa. [3] Através deste processo, os cromossomos podem ser organizados em um cariograma de 23 pares e quaisquer anormalidades envolvendo aneuploidia e grandes translocações pode ser identificado.
O cariótipo pode apenas identificar alterações em aproximadamente 3 megabases [3]. Qualquer anormalidade envolvendo menos que isso não será detectada pelo cariótipo de rotina. Pode ser usado para identificar a síndrome de Down e a síndrome de Turner.
Cariótipo para síndrome de Down
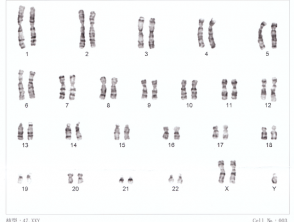
XXY cromossomos humanos
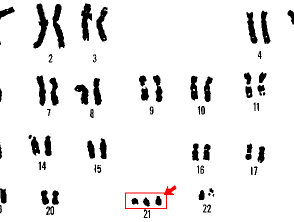
Síndrome de Trissomia Down 21
Hibridização fluorescente in situ
A hibridação fluorescente in situ (FISH) foi introduzida pela primeira vez no final dos anos 80 e rapidamente se tornou um teste citogenético diagnóstico bem conhecido em doenças congênitas e adquiridas. [5] O FISH tem uma resolução muito mais alta que o cariótipo de rotina [3], principalmente quando usado em células interfásicas [6].
O FISH usa sondas fluorescentes com seqüências de bases complementares para localizar a presença ou ausência de porções específicas de DNA nos cromossomos. [1,4] A sonda e o DNA alvo devem ser desnaturados com calor ou produtos químicos para quebrar as ligações de hidrogênio no DNA e permitir a hibridação após a mistura das 2 amostras. [6] As sondas fluorescentes formam novas ligações de hidrogênio com seus pares de bases complementares no DNA, e isso pode ser detectado por microscopia. [6]
O FISH é comumente usado para detectar deleções ou translocações cromossômicas específicas associadas a pediátrico condições ou cânceres [1]. Exemplos incluem a exclusão do cromossomo 22 na síndrome de DiGeorge e translocação a partir de um gene no cromossomo 22 e 9 em crônica mielóide leucemia [1].
O FISH também é usado para melanocítico lesões para distinguir atípico melanocítico naevi (por exemplo, Spitz nevo) Desde a maligno melanoma. Adicione uma breve descrição desse uso e outros relevantes para a dermatologia.
Hibridização fluorescente in situ no melanoma infantil
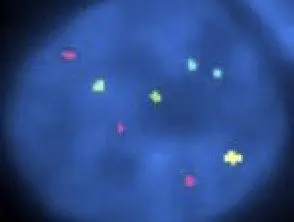
Patologia dos peixes do melanoma infantil
Hibridação genômica comparativa
A hibridação genômica comparativa (CGH) é um método de molecular Teste citogenético que detecta variantes do número de cópias cromossômicas sem a necessidade de cultura celular [7]. Foi desenvolvido para identificar essas alterações nos tumores [7,8].
CGH usa 2 genomas; a amostra de teste e um ao controle, que são marcados com fluorescência para diferenciar os dois [8]. As duas amostras são desnaturadas e misturadas, permitindo a hibridação dos cromossomos da metáfase. A intensidade do sinal fluorescente do DNA de teste marcado em relação ao DNA de controle pode ser representada ao longo de cada cromossomo, mostrando a perda ou ganho de material genético e permitindo a identificação de qualquer número de cópias. [8]
A CGH difere de outros métodos de teste citogenético, pois não se baseia em um objetivo específico, nem requer conhecimento prévio da região em análise [8]. Em vez disso, o CGH pode digitalizar rapidamente um genoma para esses desequilíbrios cromossômicos [8] e é útil nos casos em que o diagnóstico é desconhecido. Uma limitação do CGH é o tamanho da alteração genética que ele pode identificar; a resolução do CGH é baixa em aproximadamente 5 a 10 megabases [8].
Hibridação genômica comparativa
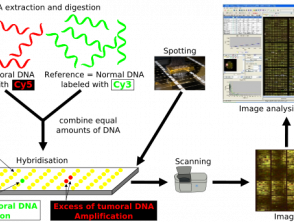
Protocolo de hibridação genômica comparativa de matrizes
Quando esse método é usado em dermatologia?
O Microarray CGH usa uma técnica semelhante ao CGH, mas fornece uma resolução muito maior ao usar microarrays [8] Pequenas seções de DNA são usadas como alvos para análise; estas seções são imobilizadas em sólido suporte [8]. Como no CGH, a amostra de DNA e o controle são marcados com fluorescência para diferenciá-los. As amostras são misturadas e adicionadas ao microarray, onde competem para se ligar às sondas no microarray [8]. A intensidade dos diferentes sinais fluorescentes pode ser avaliada e pequenos ganhos ou perdas no DNA são identificados. Uma desvantagem do microarray CHG é que ele não pode detectar alterações estruturais cromossômicas balanceadas, como translocações ou inversões balanceadas. [1].
Quando são indicados os testes citogenéticos?
Testes citogenéticos são usados quando há suspeita de anormalidade genética.
Pré-natal testes em uma gravidez de alto risco
Os testes citogenéticos são realizados em amostras obtidas no útero através da amniocentese ou pela amostragem de vilosidades coriônicas identificar um feto com anormalidades cromossômicas, como trissomia 21 na síndrome de Down.
Testes de diagnóstico
Os testes citogenéticos são frequentemente usados em pediatria, na tentativa de identificar a causa subjacente de distúrbios do desenvolvimento ou defeitos congênitos. Um diagnóstico pode ser um grande alívio para as famílias das crianças afetadas e permitirá conselhos sobre manejo adequado e previsão.
Hematológico Câncer
O teste citogenético é usado em cânceres hematológicos, como leucemia mielóide crônica (LMC), em que uma translocação recíproca específica entre os cromossomos 22 e 9 resulta no cromossomo Filadélfia, presente nos casos 95%.
Quais são os contra-indicações com testes citogenéticos?
Não há contra-indicações médicas para testes citogenéticos.
O consentimento informado deve ser obtido antes da organização dos testes.
Quais são os benefícios do teste citogenético?
Os testes citogenéticos podem oferecer diagnóstico e ajudar no manejo a longo prazo de doenças relevantes. Também permite aconselhamento genético para os pais sobre o risco de futuras gravidezes e, em alguns casos, orienta o geneticista sobre a triagem de outros membros da família.
Quais são as desvantagens do teste citogenético?
Infelizmente, o teste citogenético é limitado por sua resolução. Diferentes métodos podem identificar pequenos ganhos e perdas de material genético, bem como translocações maiores, mas não permitem o teste de um único nucleotídeo variações que podem contribuir para a condição do paciente. Existe também a possibilidade de o teste citogenético identificar outras alterações cromossômicas que não estão necessariamente relacionadas à condição do paciente.
