Anuncio
Cáncer de piel
Aplicación para facilitar el autoexamen de la piel y la detección temprana. Lee mas.
Introducción
Basal célula carcinoma (BCC) es el más común malignidad en personas de ascendencia europea y es particularmente predominante en Australia y Nueva Zelanda La causa exacta de BCC es desconocida, pero ambiental y genético factores predisponer pacientes a BCC.
Recientemente, ha habido avances en la comprensión de la molecular genética de BCC heredado y esporádico. Mal funcionamiento de la vía de señalización de erizo (HH) y gene mutaciones aumentar el riesgo de BCC.
Carcinoma de células basales
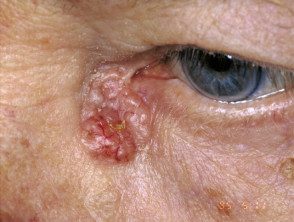
CCB noduloquístico ulcerado
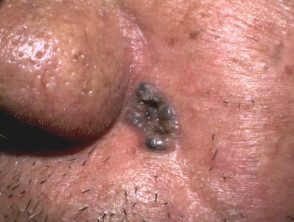
BCC pigmentado
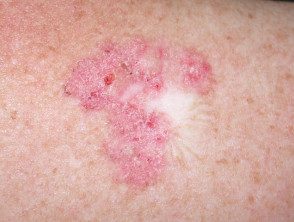
BCC superficial
¿Cuál es la ruta de señalización del erizo?
La vía de señalización de erizo (vía HH) influye en diferenciación de varios tejidos durante el desarrollo fetal.
En adultos, continúa funcionando en la regulación del crecimiento y diferenciación celular.
El mal funcionamiento de esta vía está asociado con malignidad humana, incluido el CCB.
¿Cómo funciona la vía de señalización HH?
El gen hedgehog en la ruta HH codifica una proteína extracelular, la proteína sonic hedgehog (SHH). SSH se une a la membrana celular receptor complejo para comenzar una cascada de celular eventos que conducen a la célula proliferación.
El complejo receptor de la membrana celular consta de dos proteínas:
- Proteína parcheada (PTCH) 1, el componente de unión a ligando del complejo receptor hedgehog en la membrana celular
- Proteína suavizada (SMO), responsable de transducir la señalización de hedgehog hacia abajo genes.
En el estado de reposo, PTCH1 mantiene SMO en un estado inactivo, inhibiendo así la señalización a genes posteriores.
En el estado activo:
- SHH se une a PTCH1
- PTCH1 inhibición de SMO se lanza
- La ruta del hedgehog se activa a través de una serie de proteínas que interactúan, incluido el supresor de la proteína fusionada (SUFU), lo que a su vez conduce a la activación de los factores de transcripción y la expresión de genes reguladores del ciclo celular objetivo.
¿Qué sucede cuando la vía HH funciona mal?
El mal funcionamiento de la vía HH se asocia con malignidad humana, incluido el CCB.
El funcionamiento normal de la vía HH puede verse afectado debido a mutaciones en los genes que codifican las proteínas PTCH1, PTCH2, SMO o SUFU.
PTCH1 Las mutaciones genéticas evitan que la proteína PTCH1 se una a SMO.
Unso SMO permite el crecimiento celular no regulado mediante la activación de lo siguiente:
- Factores de transcripción (proteínas que se unen a proteínas específicas ADN secuencias y controlar el flujo de información genética del ADN a ARN) GLI1 (asociado a glioma oncogen 1; también llamada proteína de dedo de zinc) y GLI2
- Genes de proliferación celular (ciclina D, ciclina E, myc) y
- Reguladores del proceso que implica el crecimiento de nuevos vasos sanguineos (angiogénesis)
Genes principales que aumentan el riesgo de CCB
Mutaciones en el PTCH1, PTCH2, SMO y SUFU genes predisponen a los pacientes a BCC.
Pacientes con célula basal nevo síndrome (Síndrome de Gorlin) nacen con una herencia mutación de uno alelo del PTCH1 gene. La mutación conduce a un autosómico síndrome dominante de cáncer predisposición. El alelo bueno restante puede sufrir mutación a través de UV exposición a la radiación en una vida, de modo que estos pacientes puedan desarrollar tumores de CCB a una edad más temprana que la población general.
- Hasta el 70% de las personas con CCB esporádico sin síndrome de nevus de células basales he parcheado PTCH1 mutaciones genéticas como resultado de la exposición a la radiación UV.
- En el 10-20% de los pacientes con CCB esporádico, las mutaciones en el gen SMO permiten la señalización no regulada de tumor crecimiento.
- Un pequeño número de pacientes esporádicos de BCC tienen mutaciones en el PTCH1 homologo PTCH2 (una variante de la PTCH1) y SUFU.
Otros genes de importancia en el riesgo de CCB
Mutaciones en el gen supresor tumoral P53 y el receptor de melanocortina-1 (MCR1) gen puede estar involucrado en el desarrollo de BCC esporádicos.
Gen P53
- P53 codifica la proteína P53 que se ha denominado ‘guardián de la genoma’.
- La proteína P53 funciona para detectar la lesión genotóxica y detener la división celular, lo que permite la reparación del ADN antes de la replicación.
- En el caso de daño extenso en el ADN, induce apoptosis (muerte celular) para eliminar defectos y potencialmente maligno células.
- Mutaciones de P53 ocurren en una amplia variedad de cánceres humanos, incluido BCC.
- En 44 a 100% de los pacientes con CCB, se encuentran mutaciones en P53, muy probablemente como resultado de la exposición a la radiación UV.
-
Se sabe que la exposición al arsénico contribuye a la formación de BCC y se cree que ocurre a través de la metilación del ADN de genes en el P53 ruta.
Gen del receptor de melanocortina-1
- los MC1R códigos genéticos para la proteína del gen del receptor de melanocortina-1 (MC1R) expresada en la superficie de melanocitos.
- Tras la estimulación por el α-melanocitohormona estimulante (αMSH), conduce a la producción de melanina en la piel y cabello.
- Si el MC1R El gen es de tipo salvaje, la eumelanina se produce y produce piel bronceada y cabello oscuro.
- los MC1R Las variantes del color rojo del cabello (RHC) conducen a la producción de feomelanina y RHC fenotipo: piel clara, pelo rojo, pecas y una mayor susceptibilidad a melanoma y cánceres de piel no melanoma.
- Varios estudios confirman la asociación de MC1R variantes con riesgo de CCB y muestran que una tez clara además de MC1R Las variantes aumentan enormemente este riesgo.
Genes diversos
Las mutaciones / variantes de los siguientes genes pueden predisponer a los pacientes a un CBC esporádico:
- Gen glutatión-S-transferasa (las glutatión-S-transferasas celulares están involucradas en la protección contra el estrés oxidativo en la piel)
- P 450 CYP enzima gen (citocromo P450 enzimas están involucrados en la desintoxicación de numerosos xenobióticos, incluidos cancerígeno componentes del humo del tabaco)
- Gen de reparación de ADN XRCC3
- Ciclinadependiente genes inhibidores de la quinasa CDKN2A y CDKN2B
- Basal queratinocitos bordillo K5 gene
- BRM gene.
Erizo antagonista para BCC avanzado
Vismodegib (nombre comercial Erivedge ™) es un inhibidor de la ruta del erizo que fue aprobado en 2012 para el tratamiento de pacientes avanzados y metastásico BCC En 2015, sonidegib también fue aprobado para el tratamiento del carcinoma basocelular avanzado.
Otras terapias dirigidas moléculas de la vía de señalización HH están en desarrollo.


