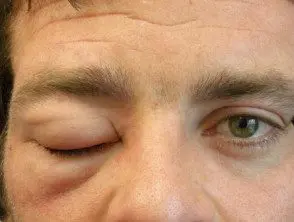
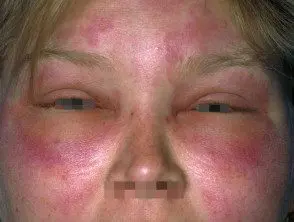
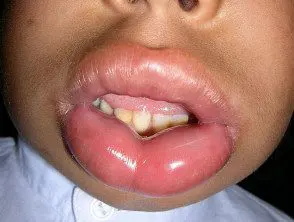
Que es hereditario angioedema?
El angioedema hereditario es un raro autosómico enfermedad dominante que se asocia con una deficiencia o disfunción de la actividad del inhibidor de la C1-esterasa (C1-INH). El angioedema hereditario causa espontáneo, recurrentee inflamación potencialmente mortal en varias regiones del cuerpo, incluida la laringe.
Angioedema
¿Qué es lanadelumab?
Lanadelumab (también llamado lanadelumab-flyo) es un medicamento biológico recetado que se usa en pacientes de 12 años o más para prevenir ataques de inflamación severa debido al angioedema hereditario. Es el primero monoclonal anticuerpo disponible para angioedema hereditario.
Lanadelumab fue aprobado por la Administración de Drogas y Alimentos de los Estados Unidos (FDA) en agosto de 2018, en Canadá en septiembre de 2018 y por la Comisión Europea en noviembre de 2018. Las solicitudes regulatorias para la comercialización de lanadelumab también se están considerando en Australia. Lanadelumab no está disponible actualmente en Nueva Zelanda.
Lanadelumab se comercializa bajo la marca Takhzyro ™ por Dyax Corp (una subsidiaria de Shire) con sede en Burlington, MA, EE. UU.
¿Cómo funciona lanadelumab?
Lanadelumab es completamente humano inmunoglobulina G1, anticuerpo monoclonal de cadena ligera kappa que proporciona inhibición de plasma calicreína, un regulador crítico de los ataques de angioedema hereditario.
- La actividad de la calicreína plasmática está regulada por la actividad de C1-INH.
- La deficiencia o disfunción de C1-INH conduce a aumentos incontrolados de la actividad de calicreína plasmática.
- La calicreína plasmática es un proteasa eso funciona dividiendo el alto molecular peso de cininógeno (a coagulación proteína) para generar el pro-inflamatorio péptido bradiquinina La bradiquinina es un potente vasodilatador y aumenta vascular permeabilidad, que es la causa de la hinchazón y el dolor asociados con el angioedema hereditario.
- Lanadelumab obstruye el proteolítico sitio activo de calicreína plasmática, evitando la división del quininógeno en bradiquinina.
- Lanadelumab, por lo tanto, disminuye la actividad de calicreína y bradiquinina en plasma en pacientes con angioedema hereditario.
¿Cuál es la indicación para lanadelumab?
Lanadelumab está indicado para prevenir ataques recurrentes de angioedema hereditario en pacientes de 12 años de edad y mayores.
- No está destinado al tratamiento de agudo ataques de angioedema hereditario.
- El tratamiento debe iniciarse bajo la supervisión de un médico con experiencia en el tratamiento de pacientes con angioedema hereditario.
¿Cómo se administra lanadelumab?
Lanadelumab puede ser autoadministrado por el paciente o administrado por un cuidador después de recibir capacitación sobre subcutáneo técnica de inyección por un profesional de la salud.
- La dosis inicial recomendada es 300 mg de lanadelumab por inyección subcutánea cada 2 semanas.
- La inyección debe restringirse a los sitios de inyección recomendados: el abdomen, los muslos y los brazos externos superiores, con el sitio de inyección girando según sea necesario.
- En pacientes que no tienen ataques de hinchazón durante el tratamiento, la dosis puede reducirse a 300 mg cada 4 semanas.
- Si se omite una dosis de lanadelumab, la dosis omitida debe administrarse lo antes posible, asegurando al menos 10 días entre dosis.
Contraindicaciones a lanadelumab
El principal contraindicación a lanadelumab es hipersensibilidad al principio activo o a cualquiera de los excipientes.
Advertencias y precauciones
Trazabilidad
Para mejorar la trazabilidad de los medicamentos biológicos, debe registrarse claramente el nombre y el número de lote del lanadelumab administrado.
Reacciones hipersensibles
Se han observado reacciones de hipersensibilidad a lanadelumab. En caso de una reacción de hipersensibilidad grave, la administración de lanadelumab debe interrumpirse de inmediato y se debe iniciar el tratamiento adecuado.
General
Lanadelumab no está destinado al tratamiento de ataques agudos de angioedema hereditario. En el caso de angioedema irruptivo, el tratamiento individualizado debe iniciarse con medicación de rescate aprobada.
No hay datos clínicos disponibles sobre el uso de lanadelumab en pacientes con angioedema hereditario con actividad normal de C1-INH.
Modificación de dosis
Pacientes con renal discapacidad
No se han realizado estudios en pacientes que toman lanadelumab que tienen insuficiencia renal grave. No se espera que la insuficiencia renal afecte la exposición a lanadelumab o su perfil de seguridad. No se requiere ajuste de dosis en pacientes con insuficiencia renal.
Pacientes con hepático discapacidad
No se requiere ajuste de dosis en pacientes que toman lanadelumab que tienen insuficiencia hepática. No se espera que la insuficiencia hepática afecte la exposición al lanadelumab. No hay estudios en pacientes con insuficiencia hepática moderada o grave.
Personas mayores
No se requiere ajuste de dosis para pacientes mayores de 65 años porque no se espera que la edad afecte la exposición al lanadelumab.
Niños
La seguridad y eficacia de lanadelumab en niños menores de 12 años no se ha establecido. No hay datos disponibles.
Uso de lanadelumab en poblaciones específicas.
Mujeres embarazadas
No hay datos disponibles sobre el uso de lanadelumab en mujeres embarazadas para informar los riesgos asociados con los medicamentos. Monoclonal anticuerpos como lanadelumab puede atravesar la placenta durante el tercer trimestre del embarazo con efectos potencialmente dañinos para el feto. Estudios de lanadelumab en embarazadas monos cynomolgus, tratado con 33 veces la dosis máxima recomendada para humanos, no reveló evidencia de daño al feto en desarrollo.
Madres lactantes
No se sabe si lanadelumab o su metabolitos se excretan en la leche humana. Debido a que muchos medicamentos se excretan en la leche humana, las madres deben suspender la lactancia antes de usar lanadelumab. Disponible farmacocinética Los datos en monos cynomolgus han demostrado la excreción de lanadelumab en la leche a aproximadamente el 0.2% del nivel plasmático materno.
Niños
No se ha establecido la seguridad y eficacia de lanadelumab en niños menores de 12 años.
Personas mayores
En ensayos clínicos, no se han observado diferencias generales en seguridad o efectividad entre pacientes mayores de 65 años y pacientes más jóvenes tratados con lanadelumab.
Individuos en edad fértil
El efecto de lanadelumab sobre la fertilidad no se ha evaluado en humanos. Lanadelumab no tuvo ningún efecto sobre la fertilidad masculina o femenina en monos cynomolgus.
¿Cuáles son las posibles interacciones farmacológicas con lanadelumab?
No se han realizado estudios dedicados de interacción fármaco-fármaco con lanadelumab. Según sus características, no se esperan interacciones farmacocinéticas con medicamentos administrados conjuntamente.
Interacción con el ensayo aPPT
- Lanadelumab puede aumentar el tiempo de tromboplastina parcial activada (aPTT) debido a una interacción con el ensayo de aPTT.
- Reactivos utilizado en la prueba de laboratorio aPTT inicia la coagulación intrínseca a través de la activación de calicreína plasmática en el sistema de activación por contacto.
- La inhibición de la calicreína plasmática por lanadelumab puede aumentar el aPTT en este ensayo.
¿Cuáles son los posibles efectos secundarios de lanadelumab?
Los efectos secundarios más comunes en pacientes que reciben lanadelumab en ensayos clínicos se describen a continuación.
Efectos secundarios con más de un 10% incidencia
A una dosis de lanadelumab 300 mg cada 2 semanas, lo siguiente Reacciones adversas donde visto:
- Reacciones en el lugar de la inyección, incluido dolor, eritemay hematomas (56%)
- Tracto respiratorio superior infección (44%)
- Dolor de cabeza (33%)
- Mialgia (11%).
A una dosis de lanadelumab 300 mg cada 4 semanas, se observaron las siguientes reacciones adversas:
- Reacciones en el lugar de inyección (45%)
- Infección del tracto respiratorio superior (31%)
- Dolor de cabeza (21%).
Efectos secundarios de 1 a 10% de incidencia
Las reacciones adversas de 1 a 10% de incidencia observadas con lanadelumab incluyen:
- Aumento de alanina transferasa (ALT) y aspartato transferasa (AST) hígado enzimas (2%)
-
Hipersensibilidad (1%): síntomas de una enfermedad grave. reacción alérgica incluir urticaria, picazón / hinchazón (especialmente de la cara, lengua y garganta), mareos intensos y dificultad para respirar.
A una dosis de 300 mg de lanadelumab cada 2 semanas, se observaron las siguientes reacciones adversas:
- Erupción (4%)
- Mareos (4%)
- Diarrea (4%).
A una dosis de lanadelumab 300 mg cada 4 semanas, se observaron las siguientes reacciones adversas:
- Sarpullido (10%)
- Mareos (10%).
Inmunogenicidad
El tratamiento con lanadelumab se ha asociado con el desarrollo de anticuerpos antidrogas en 10 de 84 pacientes (11,9%). Todos los títulos de anticuerpos fueron bajos. La respuesta de anticuerpos antidrogas fue transitoria en el 20% de los sujetos positivos para anticuerpos antidrogas; dos de 84 pacientes tratados con lanadelumab (2.4%) dieron positivo para anticuerpos neutralizantes.
El desarrollo de anticuerpos antidrogas, incluidos los anticuerpos neutralizantes contra lanadelumab, no pareció afectar negativamente a la farmacocinética y farmacodinámica perfiles o la respuesta clínica.

